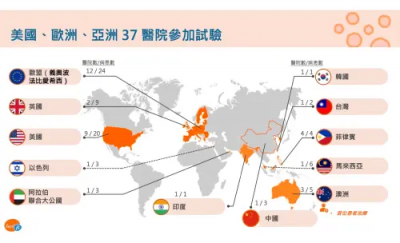
我是廣告 請繼續往下閱讀 新藥AC-203用在治療罕見疾病——「單純型遺傳性表皮分解性水皰症」(EBS,俗稱泡泡龍症)。安成生技總經理蔡承恩表示,全球第二/三期臨牀試驗(EBShield)是一項挑戰性很大的全球性試驗,在美國、歐洲、亞洲一共19個國家、37個試驗中心同步進行,如今能在全球順利完成收案,感到非常振奮,並向參與這個試驗的所有醫療團隊、受試者和家屬表達由衷的感謝。
本試驗為隨機、雙盲且與安慰劑對照的臨牀試驗,試驗期程為40週 (含療效指標分析與長期安全性追蹤)。隨著第81位受試者正式進入臨牀程序,安成生技將依計畫確實執行後續臨牀與數據統計作業,以確保臨牀數據之完整性與可靠性。
由於全球目前尚無核准用於治療EBS的專屬藥物,AC‑203可望成為全球首項獲准上市的EBS治療用藥,目前已取得美國FDA授予之孤兒藥資格認定、新藥快速審查與罕見兒科疾病資格,以及歐洲EMA及台灣TFDA授予的孤兒藥資格,顯示AC-203用在治療EBS具備重要的法規優勢。
同時,AC-203擁有向美國FDA申請「兒科罕見病優先審查憑證」的資格。該憑證可以在市場上轉讓,近年交易價格介於一至二億美元之間,享有很高的商業價值。此外,美國川普總統近日發布行政命令,對於外國專利藥品加徵100%關稅,但具有孤兒藥資格之創新藥物在特定條件下可享以關稅豁免,更凸顯AC-203於國際市場的競爭優勢與商業化潛力。
李青縈編輯記者
財經生活中心記者,如果你是想了解更多相關新聞,請往下滑動。
如果你覺得寫得不錯,請多點幾篇新聞看一看,或是幫分享連結。
如果你發現我有寫錯,請趕快告訴我!
- 安成生物
- 罕見疾病
- 泡泡龍
- 解盲
- 罕病
標題:安成罕病泡泡龍症新藥三期臨牀 今完成收案、年底解盲
地址:https://www.twetclubs.com/post/140328.html






